Ciencia y Salud
Endoscopia precoz del cáncer en el tubo digestivo
“La detección precoz de estos cánceres, lesiones todavía localizadas, superficiales, sin proliferación ganglionar linfática o metástasis, es fundamental para evitar mutilaciones orgánicas”, subraya el Dr. José Carlos Marín Gabriel, experto en endoscopia digestiva del Hospital Universitario 12 de Octubre de Madrid.
“La endoscopia de última generación tecnológica, junto a la resección de tumores de la capa mucosa o su disección en la capa submocosa, son la llave para cerrar la puerta a la temida cirugía abierta y mantener la calidad de vida de l@s pacientes”, destaca el también director científico del Instituto Clínico del Aparato digestivo (ICAdig).
Ilustración cedida por el Dr. Enrique de Madaria Pascual, gastroenterólogo del Hospital General Universitario “Doctor Balmis” de Alicante (España).
Doctor Marín, ¿por qué es tan importante detectar a tiempo con endoscopia este tipo de tumores?
“En el fondo, y en la forma, la clave está en el pronóstico de un tumor que los médicos denominamos el estadio del cáncer; es decir, cómo de avanzada está esa lesión cuando la detectamos. Lógicamente, cuanto menos haya progresado el tumor más precoz será el diagnóstico y, por tanto, obtendremos un mejor pronóstico.
En el tubo digestivo, que tiene diferentes capas, según la porción del tracto o formación anatómica analizada (mucosa, submucosa, muscular, serosa, etc.), se pueden desarrollar tumores más o menos profundos.
Como si fuera una cebolla, si el daño tumoral es superficial (capas mucosa y submucosa) podemos quitar esa parte y seguir disfrutando del resto del órgano. Cuando el daño es más profundo lo más probable es que haya que estirpar parte del tubo digestivo (esófago, estómago, intestinos delgado y grueso).
Las lesiones en las capas mucosa y submucosa tienen pocas probabilidades de avanzar hacia otras capas más profundas si el diagnóstico es temprano: se evita que las células tumorales invadan los ganglios linfáticos de la estructura de la pared afectada, los ganglios próximos al órgano y la más que futura metástasis.
Con mucha frecuencia, las metástasis provenientes del tubo digestivo acaban de visita en el hígado.
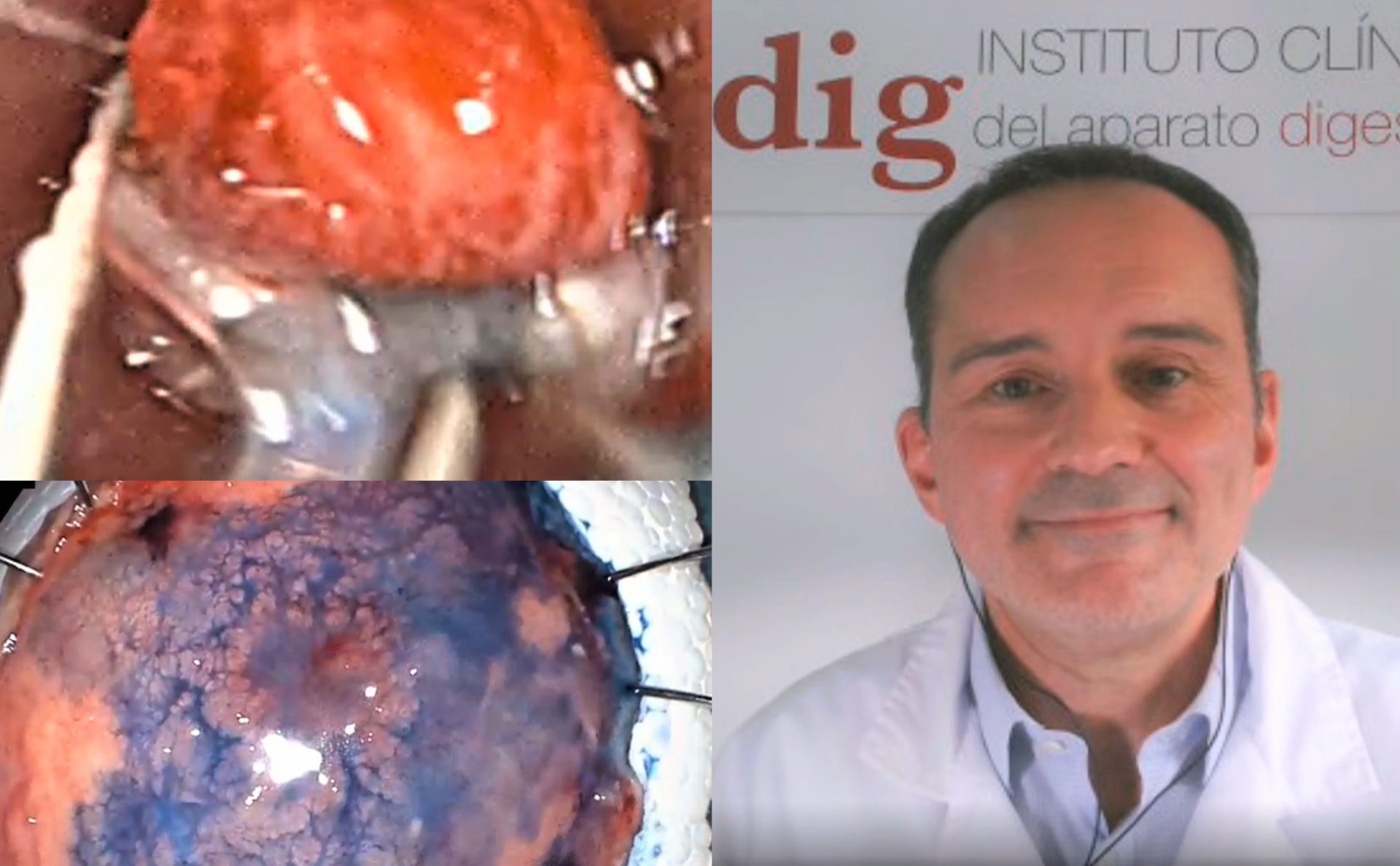
Neoplasia precoz de colon que presenta forma no granular y pseudodeprimida. Evaluación a través de cromoendoscopia, colorante índigo, magnificación y tinte de violeta genciana. La zona central de esa lesión, deprimida, demuestra un mayor potencial de células malignas. Imágenes cedidas por el Dr. José Carlos Marín Gabriel.
En resumen, detectar precozmente un cáncer en estadios primarios, en los que las células cancerosas generalmente están limitadas a las capas superficiales mucosa y submucosa, nos permite una intervención mínimamente invasiva.
En esta etapa es posible eliminar completamente el tejido canceroso mediante procedimientos endoscópicos avanzados, como la resección mucosa endoscópica (EMR) y la disección submucosa endoscópica (ESD).
Estos tratamientos reducen significativamente la necesidad de cirugías mayores, que podrían implicar la extirpación parcial o total del órgano afectado.
La extirpación de órganos como el estómago, el esófago o partes del colon puede tener consecuencias muy significativas y determinante en la digestión y la nutrición del paciente.
Al tratar el cáncer en sus primeras etapas, se mejora notablemente la calidad de vida del paciente, ya que, como hemos dicho, se preserva la funcionalidad del órgano.
Además, la detección temprana del cáncer en el tracto digestivo se asocia a tasas de supervivencia mucho más altas. Cuando el cáncer se diagnostica y trata en una etapa precoz las probabilidades de curación son mayores y el riesgo de que vuelva a desarrollarse (recurrencia) disminuye.
Por estas razones, es fundamental fomentar la concienciación sobre los signos y síntomas del cáncer digestivo y promover la realización de cribados regulares en poblaciones de riesgo: antecedentes familiares de cáncer digestivo o con condiciones predisponentes, como el esófago de Barrett o la enfermedad inflamatoria intestinal.
Trabajo endoscópico para señalizar el perímetro de una neoplasia epidermoide de esófago que va a ser tratada con disección de la capa submucosa. Visión cromoendoscópica.
Doctor, vayamos por partes. ¿Cuáles son los métodos de diagnóstico precoz en el cáncer epidermoide de esófago?
El cáncer epidermoide de esófago es una forma de cáncer que se origina en las células que recubren la capa interna del esófago. La capa más interna del esófago tiene un tipo de recubrimiento especial que llamamos epitelio escamoso.
Este epitelio escamoso es como la piel, con varias capas de células planas, pero sin que tenga queratina en su superficie (la capa proteica que la protege y la hace más resistente e impermeable).
Para diagnosticarlo de manera precoz, la endoscopia es el método de elección porque permite detectar lesiones mínimas que no serían visibles con métodos de imagen convencionales como la radiografía o la tomografía computarizada.
La mejor forma de ver estas lesiones, muy sutiles en su mayoría, es empleando técnicas de cromoendoscopia y magnificación.
Los tumores precoces se ven más oscuros que la mucosa sana con NBI (imagen de banda estrecha para visualizar en detalle la superficie mucosa y su patrón vascular) o BLI (luz azul verdosa). Cuando se usa disolución de Lugol como colorante las lesiones se ven amarillentas o rosadas.
Además, con magnificación, y viendo el dibujo de sus vasos superficiales, podemos predecir hasta dónde ha llegado la tumoración en las capas de la pared y dirigir al paciente hacia un tratamiento endoscópico con intención curativa… o a cirugía si vemos que el patrón es muy sugestivo de invasión profunda.
La identificación temprana de estas lesiones permite intervenir antes de que el cáncer haya invadido profundamente la pared esofágica o se haya diseminado a otros órganos.
Esta detección temprana es fundamental porque, en sus etapas iniciales, el cáncer epidermoide de esófago puede ser tratado eficazmente con técnicas endoscópicas, como la resección mucosa o la disección submucosa, evitando la necesidad de cirugías más invasivas y preservando la integridad del esófago.
En el esófago, además, evitar una cirugía es fundamental dado que las intervenciones quirúrgicas en esta zona suelen ser muy complejas y, con frecuencia, dan lugar a muchas complicaciones postoperatorias.
Por supuesto, la detección precoz tiene un impacto significativo en el pronóstico del paciente.
Los cánceres esofágicos en etapas avanzadas tienen un pronóstico pobre debido a la dificultad de tratamiento y la alta probabilidad de diseminación metastásica. Sin embargo, cuando se detectan en etapas tempranas, las tasas de supervivencia a largo plazo mejoran considerablemente.
Es fundamental destacar que las personas con factores de riesgo, como el tabaquismo, antecedentes de tumores en la cabeza y el cuello, consumo excesivo de alcohol, o lesiones en el esófago, incluso si son antiguas y resultaron de la ingesta de ácidos o sustancias alcalinas (cáusticos), deben someterse a exámenes endoscópicos regulares.
Estos exámenes son cruciales para la detección temprana y el tratamiento oportuno del cáncer, lo que puede mejorar significativamente el pronóstico y la calidad de vida del paciente.
Doctor, ¿cómo se diagnostica precozmente el adenocarcinoma de Barrett?
El adenocarcinoma sobre Barrett es un tipo de cáncer que se desarrolla en el esófago de Barrett.
Cuando hablamos del reflujo gastroesofágico, comentamos que el Barrett es una condición en la cual el revestimiento normal del esófago es reemplazado por un tipo de tejido similar al del intestino debido al daño crónico por reflujo ácido.
Esta metaplasia intestinal aumenta el riesgo de desarrollar adenocarcinoma, un cáncer que surge de las células glandulares presentes en el tejido de la mucosa de Barrett.
Para el diagnóstico precoz del adenocarcinoma sobre Barrett, la vigilancia endoscópica regular es esencial. L@s pacientes con esófago de Barrett deben someterse a endoscopias de revisión, durante las cuales se toman biopsias de forma muy protocolizada.
Pero lo más importante es dedicar tiempo a mirar muy bien, con un endoscopio de alta definición, todo el segmento de esófago afectado: la probabilidad de que haya displasia sobre el Barrett (que luego puede degenerar en un cáncer) depende de lo largo que sea. A mayor longitud, mayor probabilidad de displasia.
Identificar y tratar la displasia en sus primeras etapas es clave para evitar el desarrollo de un cáncer invasivo.
El endoscopista debe fijarse en irregularidades o cambios de color. Sobre esos, se enfocará detalladamente buscando irregularidades en las glándulas que forman el Barrett y en sus vasos. Cuanto más irregulares ambos, más probablemente estaremos viendo una lesión precoz.
Además, podemos usar técnicas de cromoendoscopia y magnificación para visualizar mejor esas áreas sugestivas de displasia.
La detección precoz mediante endoscopia tiene múltiples beneficios. En primer lugar, permite intervenir antes de que el cáncer se encuentre en un estadio más avanzado.
En las etapas iniciales, el adenocarcinoma puede tratarse de manera efectiva con procedimientos endoscópicos como la resección mucosa o la disección submucosa, que eliminan el tejido displásico o el cáncer precoz sin necesidad de cirugía mayor.
De nuevo, evitar cirugías en el esófago es muy importante, debido a las complicaciones graves que puede inducir.
Como con cualquier otro cáncer precoz en el tubo digestivo, el tratamiento endoscópico mínimamente invasivo tiene excelentes tasas de supervivencia y mejora la calidad de vida de los pacientes con esófago de Barrett.
Doctor Marín Gabriel, en el anterior videoblog hablamos del cáncer de estómago, ¿pero cómo es su diagnóstico precoz?
El cáncer gástrico precoz se caracteriza por estar limitado a sus capas de mucosa y submucosa, independientemente de si hay o no diseminación a ganglios linfáticos. El estómago es, de hecho, el origen del concepto de cáncer precoz.
Por supuesto, la endoscopia es la herramienta principal para identificar el cáncer gástrico precoz.
En países como Japón, que tiene una alta incidencia de cáncer gástrico, y donde el cribado endoscópico es una práctica común, se ha logrado detectar una alta proporción de cánceres gástricos en etapas precoces, lo que ha llevado a una mejora notable en las tasas de supervivencia.
En nuestro medio europeo no se realiza cribado de cáncer gástrico en la población dado que somos un país de baja incidencia en cáncer gástrico, si nos comparamos con otros países del mundo.
La imagen endoscópica del cáncer precoz es la de una lesión en la mucosa del estómago de forma irregular y de coloración distinta al del resto de la mucosa sana.
Para estudiar detalladamente estos tumores conviene emplear endoscopios de magnificación y cromoendoscopia.
Se presentan como una irregularidad en los vasos y en las glándulas de superficie en el interior de lo que llamamos un área demarcada (una zona bien delimitada que es diferente al resto de la mucosa que la rodea).
El diagnóstico precoz del cáncer gástrico ofrece varias ventajas.
En primer lugar, permite el uso de tratamientos endoscópicos como la resección mucosa y la disección submucosa, que pueden extirpar el tumor sin la necesidad de una gastrectomía, es decir, sin la extirpación de parte o de todo el estómago.
Esto preserva la función gástrica y mejora la calidad de vida del paciente.
Además, el cáncer gástrico en etapas tempranas tiene una probabilidad significativamente menor de haber metastatizado a los ganglios linfáticos, lo que hace que los tratamientos locales sean más efectivos y aumente la posibilidad de una cura completa.
En resumen, la endoscopia es una herramienta esencial en la lucha contra el cáncer gástrico precoz, permitiendo una detección temprana y un tratamiento oportuno.
Doctor, ¿es posible realizar un diagnóstico precoz el cáncer en el intestino delgado con endoscopia?
Los tumores del intestino delgado son muy, pero que muy infrecuentes. Los más habituales son los adenomas duodenales. Se encuentran en la zona que vemos durante una gastroscopia al pasar el anillo del píloro, en la primera parte del intestino delgado.
Por lo general encontramos estas lesiones durante gastroscopias que se solicitan por otro motivo. Suele ser por puro azar. Como son infrecuentes, en la población general no se hace un cribado específico de estas lesiones.
Los adenomas duodenales esporádicos, que se dan en personas sin antecedentes de poliposis adenomatosa familiar, suelen ser lesiones únicas y de curso habitualmente muy benigno.
Sin embargo, no es raro que puedan llegar a tener un tamaño importante, de más de 2 cm, y que supongan un desafío para el endoscopista.
Además, asientan en una zona del intestino donde las capas de este parte del tubo digestivo son muy delgadas y es más probable que haya complicaciones tras el procedimiento, como el sangrado y la perforación.
Y, por si fuera poco, las úlceras que dejamos en la mucosa al resecarlo, quedan expuestas al jugo biliopancreático que sale muy cerca, de la papila duodenal. Esto incrementa las posibilidades de complicaciones en la endoscopia.
La alternativa quirúrgica suele ser muy compleja y se tiende a preferir el tratamiento endoscópico, mínimamente invasivo.
En pacientes con poliposis adenomatosa familiar o en las asociadas al gen MUTYH, la probabilidad de aparición de adenomas duodenales sí que está muy aumentada. Además, suelen salir muchas lesiones y son pacientes que requieren una vigilancia muy estrecha con gastroscopias de vigilancia.
Finalmente, hay enfermedades hereditarias que pueden desarrollar pólipos en el resto del intestino delgado y vigilar esas áreas requiere otro tipo de procedimientos para ver tramos más largos del intestino delgado, como la ERM (entero resonancia magnética), la enteroscopia o la capsuloscopia.
Estos procedimientos nos ayudan a vigilar los casos de síndrome de Lynch que tienen antecedentes familiares de tumores del intestino delgado o el síndrome de Peutz-Jeghers, en el que los pacientes desarrollan pólipos en tramos distantes del intestino delgado.
Doctor Marín, ¿y cómo descubre el endoscopista los cánceres colorrectales más precoces?
No hay una definición unánime para el cáncer colorrectal precoz, pero se tiende a emplear el concepto de invasión no más allá de la submucosa profunda del colon o del recto y que no ha invadido los ganglios linfáticos ni otros órganos.
Este tipo de cáncer se encuentra también en una fase temprana, lo que permite que las opciones de tratamiento sean menos invasivas y más efectivas.
La colonoscopia es el método más eficaz para diagnosticar el cáncer colorrectal precoz, ya que permite la visualización directa del interior del colon y el recto, así como la posibilidad de extirpar pólipos y cánceres precoces durante el mismo procedimiento.
En el colon, estos tumores malignos precoces pueden presentarse como pólipos planos o pediculados. Como vimos en un videoblog previo, el tamaño y la forma de las lesiones del colon nos ayudan a predecir su probabilidad de invasión en profundidad.
En los casos más dudosos, en los que es más difícil predecir si podemos curar la lesión del paciente con endoscopia o no, usamos también endoscopios de magnificación y técnicas de cromoendoscopia virtual como el violeta de genciana.
Esta tinción nos permite ver muy bien si las glándulas están gravemente distorsionadas, lo que sugiere que el tumor ha dañado mucho la mucosa superficial y, probablemente, ya no sea una lesión precoz.
La detección precoz del cáncer colorrectal es de vital importancia porque las tasas de supervivencia son mucho más altas cuando el cáncer se trata en sus etapas iniciales.
Por supuesto, la colonoscopia regular es especialmente importante para las personas con factores de riesgo, como haber tenido previamente adenomas múltiples y grandes en el colon, los antecedentes familiares múltiples de cáncer colorrectal o enfermedades inflamatorias intestinales crónicas como la enfermedad de Crohn y la colitis ulcerosa.
La realización de cribados regulares permite identificar y tratar el cáncer antes de que se vuelva invasivo, mejorando significativamente las posibilidades de curación y reduciendo la necesidad de tratamientos más agresivos.
Doctor, durante toda la entrevista usted ha puesto el foco en la resección mucosa y la disección submucosa, ¿cómo benefician a l@s pacientes estas dos técnicas endoscópicas?
La resección mucosa endoscópica (EMR, por sus siglas en inglés) y la disección submucosa endoscópica (EMD, por sus siglas en inglés) son técnicas avanzadas utilizadas para tratar cánceres precoces del tracto digestivo sin la necesidad de realizar cirugías abiertas invasivas.
La EMR es un procedimiento en el cual se utiliza un endoscopio para extirpar lesiones cancerosas superficiales que están confinadas a la mucosa del tracto digestivo. En el caso de lesiones menores a 2 cm suele lograrse su extirpación en bloque.
Si son de mayor tamaño, se consiguen resecar en varios fragmentos.
Por otro lado, la DSE es una técnica más avanzada que permite la extirpación en bloque de lesiones más grandes, limitadas a la mucosa y submucosa, en un solo fragmento, independientemente de su tamaño.
La DSE implica la disección precisa de la submucosa bajo la lesión, es como una microcirugía, que permite una extirpación completa del tumor en una sola pieza.
Esto permite un análisis histológico adecuado y asegurar que no queden células cancerosas en el sitio de la lesión.
La DSE es técnicamente más compleja porque requiere un mayor nivel de habilidad y necesita de un largo tiempo de aprendizaje por parte del endoscopista.
Aunque ofrece la ventaja de reducir las recurrencias (reaparición de la lesión en la misma zona) no hay aún estudios que hayan demostrado mejoría en la supervivencia, menores complicaciones o mejor calidad de vida, en comparación con la RME que, técnicamente es más sencilla de realizar.
En el colon, además, la DSE suele ser un procedimiento de significativa mayor duración y está gravado con un porcentaje algo mayor de perforaciones, aunque la mayoría son milimétricas y pueden tratarse durante el mismo procedimiento endoscópicamente, cerrándolas con clips, en algunos casos pueden precisar de cirugía.
Cuando optamos por la DSE en el colon, seleccionamos mucho el tipo de lesiones que se pueden beneficiar, dado que conlleva un pequeño aumento del riesgo de complicaciones para los pacientes.
Solemos realizar esta técnica en lesiones donde el límite con la necesidad de una cirugía esté acorde con lo que más beneficia a un paciente y siempre con la intención de evitar una intervención quirúrgica que sería la alternativa tradicional.
En todo caso, estas técnicas benefician enormemente a los pacientes porque son menos invasivas, tienen tiempos de recuperación más cortos y reducen las complicaciones asociadas con las cirugías tradicionales.
Además, al preservar la integridad del órgano afectado, mejoran la calidad de vida postoperatoria del paciente.
La RME y la DSE son especialmente valiosas porque permiten la curación completa del cáncer en etapas tempranas, cuando la probabilidad de metástasis linfáticas es baja.
Esto significa que los pacientes pueden evitar cirugías más agresivas y los riesgos asociados con la extirpación parcial o total del órgano afectado.
¿Y cuáles son los factores de riesgo comunes para estos cánceres precoces del tracto digestivo?
Los factores de riesgo comunes para los cánceres del tracto digestivo incluyen una combinación de factores genéticos, ambientales y de estilo de vida.
El tabaquismo es uno de los principales factores de riesgo, ya que las sustancias químicas en el tabaco pueden dañar el revestimiento del tracto digestivo y aumentar el riesgo de cáncer, tanto en el esófago como en el estómago o el colon.
El consumo excesivo de alcohol también está asociado con un mayor riesgo de cáncer de esófago, gástrico y colorrectal.
Asimismo, ciertas infecciones crónicas, como la que provoca la bacteria Helicobacter pylori en el estómago, están vinculadas con un mayor riesgo de cáncer gástrico debido a la inflamación y el daño celular que pueden causar.
La obesidad es otro factor de riesgo significativo, especialmente para el cáncer colorrectal. El exceso de grasa corporal puede alterar los niveles hormonales y favorecer la inflamación crónica, lo que puede promover el desarrollo de células cancerosas.
Una dieta rica en carnes rojas y procesadas (salchichas, bacon, embutidos, etc.) también parece estar asociada con un mayor riesgo de cáncer colorrectal. Esta relación entre dieta y cáncer es más importante con las carnes procesadas.
En términos de factores genéticos, tener antecedentes familiares de cáncer digestivo aumenta el riesgo individual.
Condiciones hereditarias como el síndrome de Lynch y la poliposis adenomatosa familiar (FAP) están asociadas con un riesgo significativamente mayor de desarrollar cáncer colorrectal a edades tempranas.
En general, comprender y gestionar estos factores de riesgo a través de cambios en el estilo de vida, vigilancia médica y cribados regulares es esencial para la prevención y detección temprana de los cánceres del tracto digestivo.
Doctor, una última pregunta: ¿Qué recomendaciones puede dar a l@s pacientes sobre la detección precoz de estos cánceres del tubo digestivo?
Para la prevención y detección precoz de los cánceres del tracto digestivo es fundamental adoptar un enfoque que incluya cambios en el estilo de vida, cribados periódicos y vigilancia médica.
En primer lugar, llevar una dieta saludable y equilibrada puede reducir significativamente el riesgo de cáncer digestivo. Se recomienda una dieta rica en frutas, verduras y fibra… y baja en carnes procesadas.
Además, evitar el tabaquismo y el consumo de alcohol es crucial para la prevención de estos cánceres. El tabaco y el alcohol contienen sustancias químicas que pueden dañar el ADN y promover el desarrollo de células cancerosas.
Mantener un peso saludable a través de una dieta equilibrada y ejercicio regular también es importante, ya que la obesidad está relacionada con un mayor riesgo de varios tipos de cáncer digestivo, incluyendo el cáncer colorrectal.
En cuanto al cribado, en nuestro país está establecido el de cáncer colorrectal. En personas de más de 50 años, sin ningún otro riesgo, está recomendada la realización de la prueba de sangre oculta en heces.
Por lo que respecta a la vigilancia en personas con lesiones predisponentes, si hay antecedentes familiares de cáncer digestivo, esófago de Barrett, enfermedad inflamatoria intestinal o lesiones precursoras gástricas deben seguir las recomendaciones de su médico para la vigilancia regular.
Consultar a un especialista en gastroenterología y seguir sus consejos sobre el manejo de factores de riesgo y la realización de pruebas de detección es crucial para la prevención y detección temprana de estos cánceres.
En conjunto, estas estrategias pueden mejorar significativamente la detección precoz y el tratamiento de los cánceres del tracto digestivo, reduciendo la morbilidad y mejorando la supervivencia a largo plazo.
En el próximo videoblog de Aparato Digestivo viajaremos al interior del tubo digestivo de las manos expertas del Dr. José Carlos Marín Gabriel, quien nos mostrará mediante un endoscopio todas las porciones del tracto digestivo, los puntos de conexión entre ellas, sus características principales y las lesiones más frecuentes.
La entrada Endoscopia precoz del cáncer en el tubo digestivo se publicó primero en EFE Salud.
Ciencia y Salud
Los fármacos antiobesidad se asocian a un menor riesgo de cáncer en personas obesas
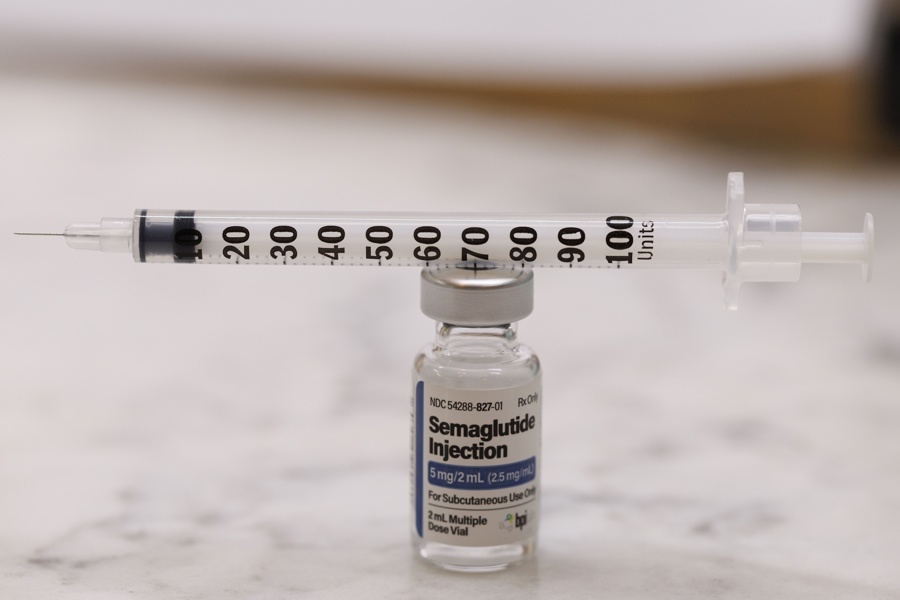

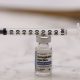
Un estudio dirigido por la Universidad de Indiana (EE.UU.) revisó las historias médicas de 42.317 personas que tomaban estos fármacos antiobesidad, los agonistas del receptor del péptido similar al glucagón-1 (GLP-1RA), como Ozempic o Wegovy, con las de un número parecido de individuos que no los usaban, para estudiar el riesgo de cáncer.
El consumo de GLP-1RA “se asoció significativamente con una reducción del riesgo de cáncer en general, en particular de cáncer de endometrio, meningioma y ovario”. Sin embargo, también se asociaron “con un aumento no significativo del riesgo de cáncer de riñón”, señala la investigación.
Los GLP-1RA se recetan ampliamente para el control glucémico en la diabetes tipo 2 y recientemente han ganado popularidad para el control del peso, pero su impacto a largo plazo sobre el riesgo de cáncer sigue siendo incierto, lo que llevó al equipo a plantearse este estudio.
El objetivo era comparar la incidencia de 14 tipos de cáncer, en concreto el de pulmón y otros trece que están asociados a la obesidad: hígado, tiroides, páncreas, vejiga, colorrectal, riñón, mama, endometrio, meningioma, tracto gastrointestinal superior, ovario, mieloma múltiple y próstata.
Las tasas de incidencia de todos ellos, entre medicados y no, fueron de 13,6 frente a 16,4 por cada 1.000 personas-año, respectivamente, “lo que indica un riesgo global de cáncer significativamente menor entre las personas que tomaban GLP-1RA”, escriben los autores.
En particular, el uso de esta familia de fármacos antiobesidad se asoció con una reducción del riesgo de cáncer de endometrio, ovario y meningioma.
Sin embargo, también se relacionó “con un aumento marginalmente no significativo del riesgo de cáncer de riñón”, lo que pone de relieve la necesidad de “un seguimiento a más largo plazo para aclarar los mecanismos subyacentes y las implicaciones clínicas de estos hallazgos”, concluye el artículo de la Universidad de Indiana.
La entrada Los fármacos antiobesidad se asocian a un menor riesgo de cáncer en personas obesas se publicó primero en EFE Salud.
Ciencia y Salud
Niños infectados por covid en el embarazo, antes de las vacunas, presentan retrasos en el desarrollo cognitivo


Esta es la principal conclusión de una novedosa investigación sobre los efectos en los niños de la pandemia de covid durante el embarazo, que ha sido liderada por el Instituto de Neurociencias del Centro Superior de Investigaciones Científicas (CSIC), el mayor centro español con fondos públicos dedicado al estudio del cerebro, con sede en Sant Joan d’Alacant (Alicante) y gestionado con la Universidad Miguel Hernández (UMH) de Elche.
Encabezado por el grupo de Neurobiología de Enfermedades Mentales de este centro mixto del CSIC y la UMH, la investigación fue publicada en la revista Cellular and Molecular Life Sciences en 2023 y sus resultados han sido respaldados a lo largo de este año 2025 en diversos estudios de científicos de varios países, cuando los niños y niñas infectados en el vientre materno rondan hoy día el lustro de vida.
La semana 20 del embarazo es un periodo fundamental en la formación de la corteza cerebral y clave para el posterior proceso de aprendizaje de las personas, ha explicado a EFE el científico principal, el neurocientífico Salvador Martínez, en cuya investigación han participado, entre otros, los murcianos José Manuel Hernández López y Cristina Hernández Medina.
La migración de neuronas y el flujo de oxígeno en esta fase crucial para el cerebro corresponde a la proteína ACE2, que a su vez se ha demostrado receptor del coronavirus, dejando entrar al SARS-CoV-2 en unas neuronas aún inmaduras porque carecen de la barrera protectora hematoencefálica, ya presente en la etapa posterior.

Efectos sobre la memoria
Al analizar varios cerebros humanos de fetos de 20 semanas de gestación donados anónimamente tras un aborto espontáneo en 2020, se ha observado que la presencia del virus de la pandemia tiene efectos “de forma muy particular y localizada en unas células de la región embrionaria del hipocampo: la parte del cerebro que se dedica a la memoria”.
De esta forma, cuando hubo infección congénita de SARS-CoV-2 y la madre tuvo que ser hospitalizada (los casos con más carga viral) se elevó la probabilidad de alteración del desarrollo cerebral, lo que puede asociarse a la aparición de trastornos del espectro autista (TEA), déficit de atención, hiperactividad y otras problemáticas del aprendizaje no asociados a un síndrome o casuística concreta, lo que se conoce como discapacidad intelectual no sindrómica.
En varios estudios epidemiológicos publicados recientemente se ha observado un aumento del 10 % del déficit cognitivo del desarrollo intelectual, comparado con datos de bebés nacidos antes y después “en los mismos lugares y en condiciones similares”, según Martínez, quien ha aclarado que esos retrasos cognitivos cayeron en los hijos de las madres ya vacunadas, por la menor carga viral.
Estos estudios amplían el conocimiento de los efectos de un SARS-CoV-2 que “infectó a toda la sociedad” sin ser tan virulento como otros virus anteriores como el de la viruela, y reflejan que en los casos en los que llegó al cerebro del feto para infectar a las células en desarrollo “se podría predecir o anticipar un aumento de la discapacidad intelectual, del retraso del desarrollo cerebral”.
“Eso es lo que ahora se puede empezar a comprobar porque esos niños tienen más de cinco años y es cuando esa región del cerebro es necesaria para que aprendan adecuadamente”, ha añadido el científico del Neurociencias.
Catedrático y profesor en París antes de director del Neurociencias
Catedrático de Anatomía y Embriología Humana en la UMH, Martínez Pérez (Abengibre, Albacete, 1961) ha desarrollado una larga carrera docente e investigadora donde ha sido profesor de l’École Doctorale de l’Institut Pasteur de París y cuenta con colaboraciones internacionales y estancias en centros extranjeros al margen de dirigir, entre 2016 y 2020, el Instituto de Neurociencias.
Además de esta investigación en niños infectados en 2020 por covid en el embarazo, su trabajo ha trascendido en otros campos como un ensayo pionero en humanos y con unos primeros resultados esperanzadores para una terapia que ralentice e, incluso, detenga la degeneración muscular de la Esclerosis Lateral Amiotrófica (ELA) con células del propio paciente extraídas de la médula ósea.
También ha dirigido recientemente un estudio que usa los ‘dientes de leche’ recién caídos de los niños como fábrica de células neuronales para terapias personalizadas dirigidas a los pequeños con enfermedades raras del sistema nervioso como el autismo, las leucodistrofias o el síndrome de Rett.
La entrada Niños infectados por covid en el embarazo, antes de las vacunas, presentan retrasos en el desarrollo cognitivo se publicó primero en EFE Salud.
Ciencia y Salud
Dátiles: nutritiva dulzura y moderado consumo


“Son tantas las propiedades de los dátiles, que ya desde la antigüedad, árabes, griegos, hebreos y egipcios, llamaban a la palmera datilera, que es el árbol del que proceden, el ‘árbol de la vida”, señala Laura Sánchez, experta en nutrición del Hospital Universitario La Luz Quirónsalud.
El Ministerio de Agricultura, Pesca y Alimentación español (MAPA) explica que a raíz de las propiedades nutritivas de los dátiles, los fenicios llamaban a la palmera datilera ‘el árbol de Dios’, ya que se podía sobrevivir viajando por el desierto con un puñado de estos frutos, los cuales llegaron a América durante la colonización con las migraciones españolas.
La palmera datilera o palmera real (Phoenix dactylifera) es una especie notable dentro de su familia botánica, las arecáceas. Puede alcanzar los 20 metros de altura, tiene un tronco de 30 a 40 centímetros de anchura, está presente de forma natural en el norte de África y suroeste de Asia, y es cultivada en las riberas septentrionales del Mar Mediterráneo.
Su origen se atribuye al Norte de África y a Asia, aunque los historiadores no se ponen de acuerdo sobre este punto.

Alto contenido en vitaminas, minerales, fibra y azucares
La nutricionista Laura Sánchez señala que los dátiles destacan por su contenido en vitaminas y minerales.
“Son frutos ricos en potasio y magnesio, dos sustancias importantes para el sistema nervioso; en niacina (vitamina B3), que ayuda a mantener sanos el sistema nervioso, el aparato digestivo y la piel; y en fibra alimentaria, sustancia vegetal que contribuye a prevenir el estreñimiento; además de ser una buena fuente de energía”, puntualiza.
La morfología del dátil es ovalada y cuenta con una semilla interior y una pulpa pegajosa de color anaranjado marronáceo, todo envuelto en una piel brillante, según lo describe la experta del HULL.
Explica que “los dátiles Medjool y Deglet Noor son las variedades más frecuentes para el consumo”, y que “contrariamente a lo que muchos piensen, el dátil no es una fruta desecada, sino que este fruto se seca ya en el propio árbol con el sol, para después ser recolectado” .
“Consumir hasta tres dátiles al día puede ser un perfecto tentempié para nuestro día a día, y lograr todos sus beneficios nutricionales”, subraya.
Precauciones y contraindicaciones
Destaca que este fruto puede ser una importante alternativa como condimento para quienes quieran endulzar sus platos de la manera más saludable, evitando los azúcares blancos o edulcorantes, aunque en el caso de padecer diabetes, se aconseja restringir su consumo.
A la hora de incorporar los dátiles a tu dieta, “debes tener en cuenta que aunque es un alimento saludable, tiene un alto contenido en azúcares, por lo que no hay que consumirlo en exceso, porque puede ser contraproducente”, advierte.
“Al ser un alimento nutritivo, con alto contenido en azúcares, los dátiles, no están indicados para personas con problemas renales y/o con problemas en la metabolización de los azúcares”, señala la nutricionista.
Sánchez indica que, al igual que ocurre con los zumos, no es igual consumir los dátiles enteros que triturados, ya que cuando se trituran, desaparece la fibra y aumenta la cantidad de azúcar en el producto final que se ingiere.

Dátiles, beneficiosos para la salud cardiovascular
El consumo moderado de dátiles puede ser beneficioso para el corazón, ya que uno de los minerales más destacados que contiene, el potasio, ayuda a reducir el riesgo de patología cardiovascular y la presión arterial, según la especialista.
Y para la piel y el cabello
Las propiedades antioxidantes de estos frutos, “favorecen la salud a la piel y el cabello, confiriéndoles un aspecto más brillante y sano; y son determinantes a la hora de reducir la inflamación del cuerpo y prevenir ciertas enfermedades”, agrega Sánchez, destacando que estos frutos son ricos en potasio, hierro, calcio, magnesio y otras vitaminas del grupo B, C y A.
Sin olvidar la microbiota, los huesos y el cerebro
Los dátiles también contienen abundante fibra, compuesto vegetal que aporta saciedad, “algo fundamental para quien quiera bajar peso”, además de mejorar la microbiota (conjunto de microorganismos beneficiosos) del intestino y nuestra salud intestinal en general; evitar el estreñimiento; y ayudar a prevenir enfermedades, incluso ajenas al tracto digestivo, puntualiza.
Estos dulces frutos destacan por su alto contenido de minerales, como magnesio, fósforo, y calcio, que claramente pueden contribuir a mantener nuestra salud ósea, añade la nutricionista.
Asimismo, “el alto poder energético y la riqueza en antioxidantes de los dátiles, pueden ayudar a reducir la inflamación en el cerebro, y a prevenir patologías neurológicas”, asegura Sánchez añadiendo que también “se sabe que el consumo de estos frutos puede favorecer una mejor función cognitiva”.
Tipos y consejos para conservar los dátiles
Laura Sánchez señala que en función de los tiempos de maduración, lo cual hace que varíen su textura y consistencia, los dátiles se clasifican en tres categorías: blandos, semisecos y secos.
Explica que “independientemente de su categoría, todos tienen un alto porcentaje de azúcares, en torno a un 60%, por lo que son una importante fuente de energía.
Por otra parte, “los dátiles blandos son los más húmedos y los que más azúcares tienen. Los semisecos son carnosos y jugosos, mientras que los secos son más duros y secos”, describe.
Además de los Medjool y Deglet Noor, los más frecuentes, “hay cientos de variedades de dátiles, con diferentes colores, formas, texturas y sabores, como Halawy, Barhi, Mozafati, Zahidi, Sukkari, Khadrawy y Hayani, así como los dátiles Piarom, también conocidos como Maryam o ‘dátiles chocolate’, que son los más caros y lujosos del mundo”, puntualiza.
Para comprar dátiles de buena calidad, Sánchez recomienda asegurarse de que “a simple vista presenten un color marrón-negro brillante y jugoso; que no estén demasiados arrugados ni secos; y que no tengan manchas blancas, que indicarían que su azúcar se ha cristalizado, ni tampoco negras, que indicarían la presencia de moho”.
Otro aspecto que “debemos tener en cuenta es que el embalaje o envase de los dátiles esté bien cerrado y sin golpear”, añade.
Respecto de cuál es la mejor forma de conservar estos frutos, señala que “los dátiles blandos y semisecos necesitan refrigeración (incluso algunas veces congelación para conseguir que duren más), mientras que los secos se pueden almacenar a temperatura ambiente”.
“Los dátiles se pueden consumir al natural o utilizar en recetas dulces y saladas. ¿A qué esperas para consumirlos?”, concluye.
La entrada Dátiles: nutritiva dulzura y moderado consumo se publicó primero en EFE Salud.
-

 Newswire3 días
Newswire3 díasHONOR protege tu inversión con su programa de Garantía 360
-

 Newswire3 días
Newswire3 díasLos nuevos plegables Galaxy Z registran un crecimiento del 30% en la preventa en América Latina
-

 Newswire3 días
Newswire3 díasHuawei Cloud presenta nueva identidad visual y refuerza su posición como pionero en IA
-

 Newswire2 días
Newswire2 díasROYAL CARIBBEAN PRESENTA STAR OF THE SEAS, LAS MEJORES VACACIONES FAMILIARES
-

 Innovación y Tecnología2 días
Innovación y Tecnología2 díasGoogle revisa sus tarifas de Play Store en un intento por evitar posibles multas de Bruselas
-

 Ciencia y Salud2 días
Ciencia y Salud2 díasLos efectos en la salud del humo de los incendios puede aparecer años después
-

 Ciencia y Salud2 días
Ciencia y Salud2 días¿Por qué en verano aumentan las lesiones de espalda? 10 consejos para esquivarlas
-

 Ciencia y Salud2 días
Ciencia y Salud2 díasEn verano, protégete de los hongos en los pies con estos sencillos pasos